Les recherches d’Emmanuelle Bignon visent à élucider les mécanismes qui sous-tendent la régulation du compactage de l’ADN par des modifications post-traductionnelles, en se concentrant plus particulièrement sur les modifications oxydatives des cystéines.
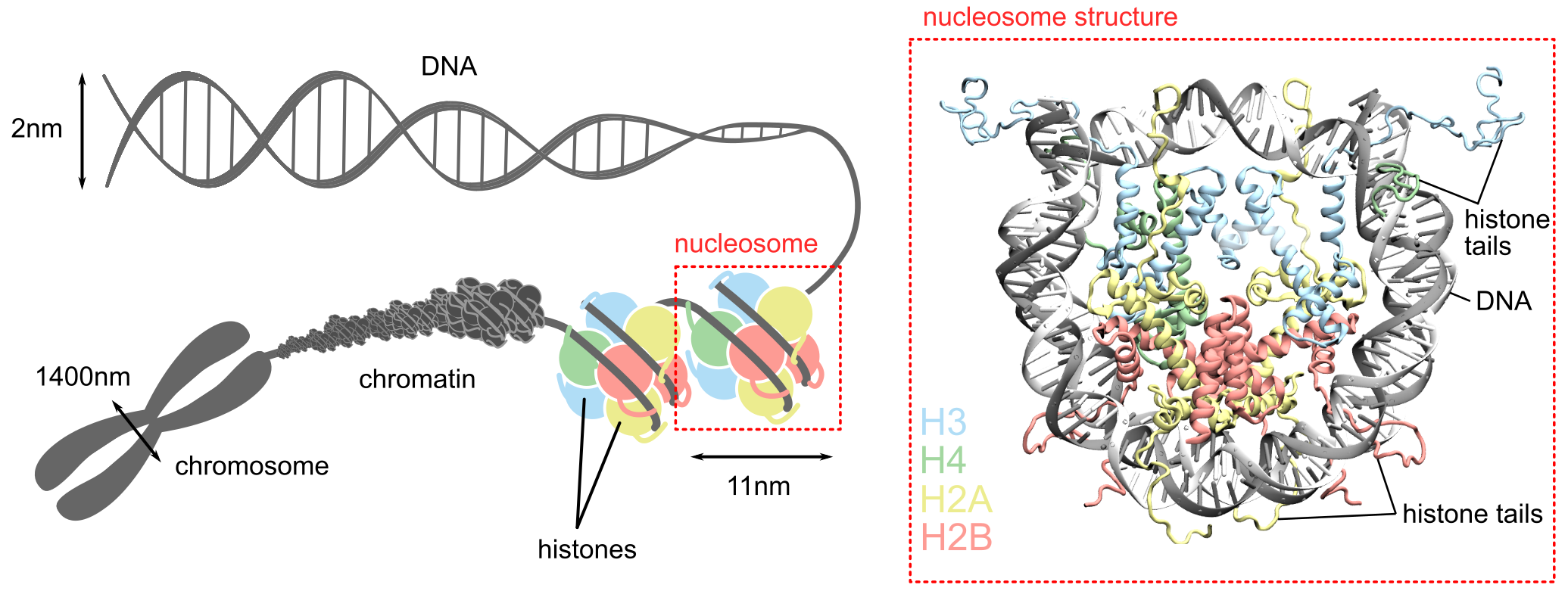
Chacune de nos cellules contient 2 mètres d’ADN, très fortement compactés dans un noyau d’environ 10 micromètres. Le premier niveau de compaction, appelé nucléosome, comprend environ 146 paires de bases d’ADN enveloppées sur un octamère de protéines histones. La dynamique de cette architecture, qui détermine l’accessibilité de l’ADN aux protéines pour l’expression des gènes et la réparation de l’ADN, est étroitement régulée par des facteurs épigénétiques tels que les modifications post-traductionnelles des histones.
Ces modifications constitueraient un « code histone » qui crypte les informations permettant de dicter le fonctionnement cellulaire via le traitement de l’ADN, dans des conditions normales ou en réponse à un stress externe. Il est bien connu que les anomalies des marques épigénétiques sont associées à de nombreuses maladies (cancer, neurodégénérescence, troubles métaboliques…), et la dernière décennie a vu une explosion d’études pour le développement d’épimédicaments et de biomarqueurs pronostiques/diagnostiques, en se concentrant particulièrement sur les traitements contre le cancer.
Dans ce contexte, les recherches d’Emmanuelle Bignon s’appuient sur une méthodologie multi-échelle faisant appel à des approches QM/MM, des simulations de dynamique moléculaire tout-atome et gros grains, pour étudier les mécanismes de formation des modifications oxydatives et leur impact sur la structure des nucléosomes et les architectures d’ordre supérieur. Ces informations sont essentielles pour acquérir une connaissance approfondie des mécanismes épigénétiques fondamentaux, afin de guider le développement de thérapies épigénétiques de nouvelle génération.